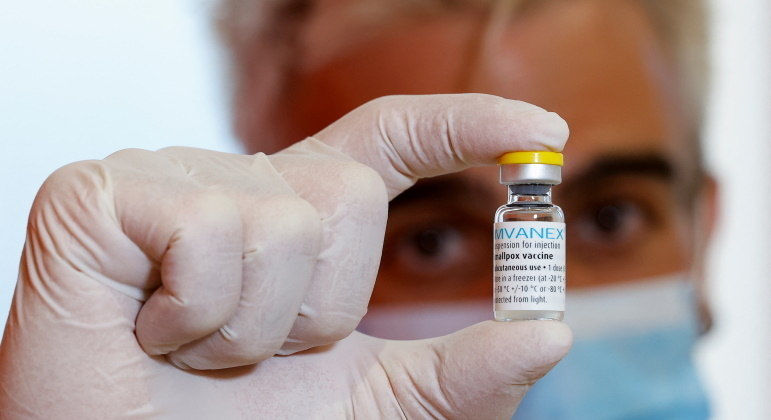
Com decisão, que é temporária, a agência acelera a aprovação de fármacos para conter a monkeypox
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou por unanimidade, nesta sexta-feira (19), a dispensa de registro e importação de medicamentos e vacinas para tratamento e prevenção contra a varíola do macaco (monkeypox), em caráter excepcional e temporário, sem a necessidade de Consulta Pública, AIR (Análise de Impacto Regulatório) e M&ARR (Monitoramento, Avaliação de Resultado Regulatório).
A regra vale para os produtos que tenham a regulamentação aprovada por autoridades sanitárias internacionais integrantes do PIC/S (Esquema de Cooperação em Inspeção Farmacêutica).
De acordo com a diretora da Anvisa, Meiruze Sousa Freitas a decisão se dá devido à necessidade de conter rapidamente a doença, já considerada emergência de saúde pública de importância internacional pela Organização Mundial de Saúde (OMS).
“Até o momento, não há, no Brasil, medicamento ou vacina registrada com a indicação de tratamento ou prevenção da monkeypox. Destaca-se também que, até o presente momento, os atuais desenvolvedores de medicamentos e vacinas para Monkeypox sinalizaram não figurar em seus respectivos planejamentos e projeções de curto prazo a intenção de submeter à Anvisa pedido de de registro ou mesmo de autorização de uso emergencial”, afirmou a diretora da Anvisa em defesa do seu voto.
Além disso, Meiruze destacou que há poucos fármacos distinado à prevenção e controle da doença.
Com a decisão, o Ministério da Saúde vai poder comprar os medicamentos e vacinas aprovadas nos países específicos e rapidamente poderá colocar à disposição da população.
O diretor-presidente da Anvisa Antonio Barras Torres salientou que a decisão não representa falta de regulamentação.
“É importante deixar claro que a Anvisa está exercendo seu papel de agência reguladora. A dispensa de registro é um ato regulatório. E esse ato não significa a aprovação tácita do que vier. Diante de mais um desafio, estamos utilizando uma ferramenta que faz parte do exercício pleno de nossa função”, observou ele.
Ministério da Saúde
Em nota divulgada nesta sexta-feira, após a decisão da Anvisa, o Ministério da Saúde afirmou que havia solicitado o registro excepcional do medicamento e do imunizante para a varíola do macaco.
“O Ministério da Saúde segue em tratativas para aquisição da vacina e medicamentos para a população brasileira junto à Organização Mundial da Saúde (OPAS/OMS) e entidades internacionais […] A decisão da agência deve acelerar a disponibilização das vacinas e tratamento no país”, diz o comunicado.
Além disso, a pasta destacou que com a evolução do cenário epidemiológico da doença no país, o Centro de Operações de Emergência em Saúde Pública (COE) foi ativado com o objetivo de organizar a atuação do SUS com a elaboração do Plano Nacional de Contingência para Monkeypox.
O Brasil tem mais de 3.450 casos da doença e já é o terceiro país do mundo com mais infectados. Está atrás apenas de Estados Unidos e Alemanha.
Fonte: Portal R7